Плотность вещества (r) – фундаментальное физическое свойства, которое определяется как отношение массы вещества к его объему: p=m/V, выражается в г/см3 (или в кг/м3).
Зависит плотность от типа кристаллической структуры вещества, его химического состава, коэффициента упаковки атомов, валентностей и радиусов слагающих его частиц.
Изменяется плотность с изменением температуры и давления, так как эти факторы вызывают расширение или сжатие вещества.
С увеличение коэффициента упаковки кристаллической структуры возрастает плотность вещества.
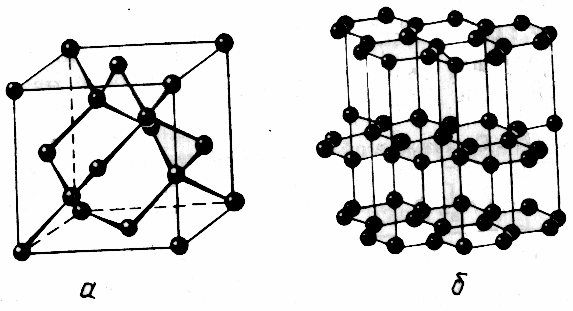
Например, при полиморфном переходе углерода графита в алмаз – с изменением координационного числа атомов углерода с 3 до 4 соответственно повышается и плотность от 2,2 до 3,5 г/см3.
Плотность реальных кристаллов обычно меньше, чем расчетная плотность (идеальных кристаллов) из-за присутствия дефектов в их структурах. Плотность алмаза, например, колеблется в пределах 2,7–3,7 г/см3. Таким образом, по уменьшению реальной плотности кристаллов можно судить о степени их дефектности.
Плотность меняется с изменением химического состава вещества при изоморфных замещениях при переходе от одного члена изоморфного ряда к другому.

(на рисунке алмаз в графите)
Твердость и температура плавления кристаллов
Твердость и температура плавления характеризуют прочность кристалла: твердость – механическую, а температура плавления – термическую прочность.
Твердость – это степень сопротивления кристалла внешнему воздействию.
Для приближенного определения твердости пользуются методом, основанном на царапании одного кристалла другим. В 1824 году австрийский минералог Ф. Моос предложил 10-балльную шкалу твердости минералов, которая позволяет приближенно оценить их твердость.

(на рисунке Ф.Моос)
Шкала твердости по Моосу
| Минерал | Относительная твердость по Моосу |
| Тальк Mg3[Si4O10](OH)2 | 1 |
| Каменная соль NaCl | 2 |
| Кальцит CaCO3 | 3 |
| Флюорит CaF2 | 4 |
| Апатит Ca5(PO4)3F | 5 |
| Полевой шпат K[AlSi3O8] | 6 |
| Кварц SiO2 | 7 |
| Топаз Al2[SiO4](F,OH)2 | 8 |
| Корунд Al2O3 | 9 |
| Алмаз C | 10 |
Твердость зависит от химического состава кристалла и от его строения: типа структуры, коэффициента упаковки, заряда образующих кристалл ионов. Например, различная твердость двух полиморфных модификаций карбоната кальция – кальцита (3 по шкале Мооса) и арагонита (4 по шкале Мооса) – объясняется различной плотностью их структур: для структуры кальцита с КЧ (Са) = 6 плотность равна 2,72 г/см3, для структуры арагонита с КЧ (Са) = 9 – 2,94 г/см3. В ряду кристаллов с одинаковой структурой твердость возрастает с увеличением заряда и уменьшением размера катиона. Присутствие больших анионов (фторид-иона, гидроксила) или молекул воды понижает твердость. Например, для изоструктурных минералов гематита Fe2O3 и корунда Al2O3 значения твердости составляют 5–6 и 9 соответственно (r(Fe3+) = 0,78; r(Al3+) = 0,57 ).
Изменение температуры плавления кристаллов связаны с изменением их твердости, чем выше твердость, тем больше температура плавления.
Замена 8-электронного иона на 18-электронный практически не влияет на изменение твердости, но значительно уменьшает температуру плавления, например: температура плавления NaCl равна 840 °С

, а AgCl – 455 °С
(оба вещества кристаллизуются в структурном типе хлорида натрия).
Твердость кристалла также зависит от грани кристалла, например для граней топаза твердость 7,5 соответствует граням пинакоида, а твердость 8 – граням призмы.
Тепловые свойства кристаллов
Теплоемкостью называется количество теплоты, необходимое для нагревания 1 моля (мольная теплоемкость) или 1 грамма (удельная теплоемкость) вещества на 1 градус.
Теплоемкость – это скалярное свойство, не зависящее от направления.
Теплопроводность – это явление переноса тепла, зависящее от симметрии кристалла.
Теплопроводность – тензорное свойство, описывается по закону эллипсоида. Если мысленно поместить точечный источник тепла внутрь кристалла и по разным направлениям отложить в виде векторов значения теплопроводности, то концы векторов образуют замкнутые изотермические поверхности в форме сферы для кубических кристаллов, эллипсоида вращения для кристаллов средней категории и трехосного эллипсоида – для кристаллов низшей категории. Таким образом, теплопроводность кубических кристаллов изотропна, а кристаллов средней и низшей категории – анизотропна.

(на рисунке карта теплопроводности)
Анизотропия теплопроводности связана со структурой кристаллических веществ. Наиболее плотным сеткам и рядам соответствуют большие значения теплопроводности, поэтому величина теплопроводности в слоистых и цепочечных кристаллах в разных направлениях различна. Например, в структуре графита теплопроводность в плоскости атомной сетки в несколько раз превышает теплопроводность в перпендикулярном слоям направлении.
Теплопроводность зависит от степени совершенства кристаллов, у более дефектных кристаллов она ниже. Аморфные вещества обладают, как правило, более низкой теплопроводностью, чем кристаллические.
Оптические свойства кристаллов
Каждое вещество с определенной кристаллической структурой обладает своеобразными оптическими свойствами. В отношении оптических свойств все вещества можно разделить на оптически изотропные и анизотропные. Изотропными свойствами обладают аморфные тела и кристаллы высшей категории, анизотропными – кристаллы средней и низшей категории.
Показатель преломления
Электромагнитные колебания естественного света происходят в плоскости, перпендикулярной направлению распространения луча. Скорость распространения света обратно пропорциональна плотности среды, поэтому при переходе света из одной среды в другую происходит преломление лучей, т. е. их отклонение от первоначального направления. Это явления характеризуется показателем преломления.
Показатель преломления – величина, показывающая во сколько раз скорость света в одной среде, отличается от скорости света в другой среде.

(на рисунке показано преломление )
Электрические свойства кристаллов
Электрические свойства кристаллов – свойства, связанные с электрической поляризацией, или самопроизвольной, или под влиянием внешних воздействий: нагревания, приложенного электрического поля, механического воздействия.
Электропроводность
Электропроводность – свойство некоторых тел проводить электрических ток. Все вещества делятся на проводящие электрический ток (проводники), полупроводники и диэлектрики (изоляторы)
В проводниках, помещенных в электрическое поле, возникает электрический ток – направленное движение заряженных частиц. Хорошими проводниками являются металлы, с повышением температуры электропроводность металлов уменьшается. В отношении электропроводности кристалл выступает как непрерывная однородная среда.
Кристаллы-диэлектрики (ионные и ковалентные) при обычных условиях не проводят электрический ток. Их можно наэлектризовать путем различных воздействий: трением, давлением, облучением, нагреванием и т. п.
Магнитные свойства кристаллов
Магнитные свойства – это способность веществ взаимодействовать с магнитным полем, т. е. намагничиваться при помещении их в магнитное поле.
В зависимости от величины магнитной восприимчивости различают:
- диамагнитные кристаллы;
- парамагнитные кристаллы;
- ферромагнитные кристаллы;
- антиферромагнитные кристаллы.
Магнитные
свойства веществ зависят те только от особенностей их кристаллической
структуры, но и от природы слагающих из частиц, то есть магнетизм
связан с электронным строением оболочек и ядер, а также орбитальным
движением вокруг них электронов.
К диамагнетикам относятся благородные газы, металлы побочных подгрупп (медь, серебро, золото и др.),

(на рисунке изображено золото)
большинство ионных кристаллов (хлорид натрия, фторид кальция и др.) и кристаллы с преобладающей ковалентной связью (сурьма, графит и др.)

(на рисунке сурьма)
При
заполнении электронных оболочек атомов электроны стремятся оставаться
неспаренными (правило Хунда), поэтому существует большое количество
веществ, магнитные моменты электронов в атомах которых расположены
беспорядочно и при отсутствии внешнего магнитного поля в них не
происходит самопроизвольная ориентация магнитных моментов. Суммарный
магнитный момент, обусловленный неспаренными электронами, будет
постоянным, положительным и несколько большим, чем у диамагентиков.
Такие атомы называются магнитными, а вещества, состоящие из таких
частиц, парамагнетиками. Например, пирит,

(на рисунке пирит)
переходные металлы: платина, титан, скандий и др.

(на рисунке платина)
При внесении таких атомов в магнитное поле разориентированные спины приобретают некоторую ориентировку, в результате чего происходит упорядочение структуры, связанное с тремя типами явлений: ферромагнетизмом, антиферромагнетизмом и ферримагнетизмом.